INFORMACIÓN BÁSICA: SIDA: Sarcoma de Kaposi (ORPHA: 33276).- El síndrome de inmunodeficiencia adquirida (SIDA) ha dejado de ser una nueva enfermedad, ya que precisamente en este nuevo milenio cumple 20 años desde su aparición. Este síndrome es consecuencia de una infección retroviral epidémica caracterizada por inmunosupresión profunda y devastadora del sistema inmune, acompañado de infecciones por gérmenes oportunistas, neoplasias secundarias y manifestaciones neurológicas.
En mayo de 1981 se conoció en los Estados Unidos este síndrome. Desde entonces se han declarado más de 500.000 casos de SIDA sólo en ese país, y han muerto más de 300.000 personas.
Actualmente existen más 1,5 millones de personas infectadas. En el Ecuador, la epidemia apareció en 1984. Desde esa fecha hasta 1999 se reportaron 2.457 casos, de estos el 49,2% son personas que viven con VIH y el 50% restante son casos de SIDA. En este período la tasa de prevalencia de VIH/SIDA se incrementó diez veces más (véase la pagina 5/Epidemiologia del SIDA en Ecuador, año 2010).
Durante el año 2.000 se detectaron en el Ecuador 663 casos, de los cuales 350 son infectados asintomáticos con VIH y 313 enfermos de SIDA, existiendo un acumulado de 1.561 infectados y 1.559 casos de SIDA reportados. Las cifras presentadas demuestran un repunte de la enfermedad, situación que amerita aunar esfuerzos y condicionar acciones tendientes a controlar el VIH/SIDA en nuestro país. Con esta prudente advertencia intentaré resumir con los datos disponibles de esta entidad, los aspectos más relevantes desde el punto de vista clínico y de laboratorio.
El SIDA está causado por el VIH, siendo este un retrovirus (perteneciente a la familia lentivirus), que contiene 9.749 nucleótidos en cada uno de sus genomas idénticos de RNA monocatenario. Utilizando la enzima transcriptasa inversa, que está presente en el virión intacto, el VIH forma una cadena complementaria de DNA monocatenario utilizando el RNA como molde y convierte el DNA complementario (cDNA) formado, en DNA bicatenario, el cual puede penetrar al genoma de la célula.
La célula diana del hospedador del VIH es la clase de linfocitos CD4 (linfocitos helper), al cual lo destruye, produciendo una disfunción del sistema inmunitario que expone a la persona infectada a diversas infecciones, comunes u oportunistas, y la predispone al desarrollo de ciertos tumores. Hay abundante evidencia de que los linfocitos CD4 son en realidad un receptor de alta afinidad para el VIH. Cerca del 5% de los pacientes infectados por el VIH comprobada no desarrollan la enfermedad progresiva. Algunos parecen estar infectados por virus mutantes que carecen de la proteína reguladora (nef), otros desarrollan una respuesta inmunológica vigorosa.
Entre las diferentes complicaciones me referí exclusivamente al angiosarcoma de Kaposi Epidémico.
Sarcoma de Kaposi Epidémico: El sarcoma de Kaposi (SK) es una neoplasia de células endoteliales linfáticas que fue descrita por primera vez en 1872. Clásicamente, se han descrito cuatro grupos que desarrollan los diferentes tipos de sarcoma de kaposi (Tabla 1). El SK clásico se presenta en pacientes de origen mediterráneo, siendo Turquía e Italia, países de alta endemicidad. Suelen presentar un curso lento y benigno. Aparece en la sexta década de la vida. La localización más frecuente es a nivel de extremidades inferiores, con afectación puramente cutánea. Puede haber afectación oral. La enfermedad ganglionar y pulmonar es poco frecuente.
El SK endémico o africano aparece en pacientes más jóvenes, entre 30-45 años. Se divide en otros subtipos como el nodular con curso clínico similar al SK clásico; algunas formas más agresivas: florida e infiltrativa y el subtipo linfadenopático que se presenta en niños y puede ser letal.
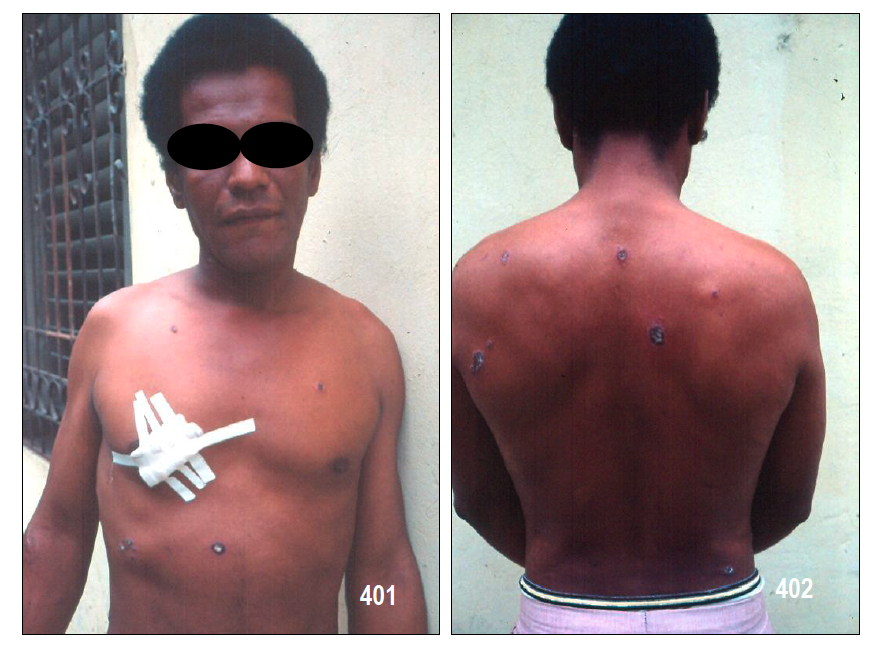
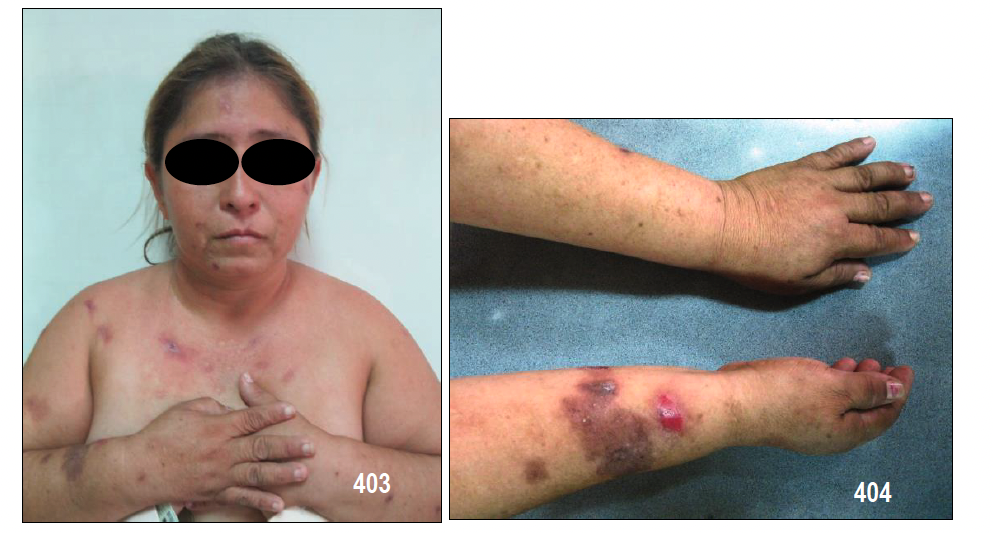
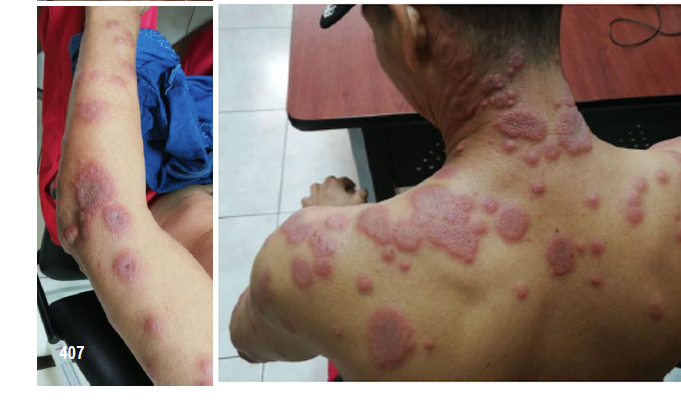
El SK epidémico o asociado a VIH es más frecuente en varones con infección por el virus de la inmunodeficiencia adquirida. Tiene predilección por la región cefálica (párpados, nariz y orejas). La afectación de mucosas es frecuente sobre todo a nivel oral (imagen adjunta) y puede ser la
manifestación inicial de la enfermedad en un 15% de estos casos. Si existe afectación en el tronco, las lesiones siguen una distribución blaschkoide. Estos pacientes pueden presentar afectación extracutáneas: gastrointestinal, pulmonar y ganglionar.
El SK yatrogénico se presenta en pacientes con compromiso de su inmunidad, ya sea por su enfermedad de base o por los tratamientos que reciben. Este tipo se observa en pacientes trasplantados, oncológicos o afectos de enfermedades inflamatorias/autoinmunes que precisen tratamientos inmunosupresores. La edad de estos pacientes es menor respecto al SK clásico. Aunque puede haber afectación ganglionar y visceral, la afectación cutánea sigue siendo la más frecuente.
•Histología: El diagnóstico de SK es histológico. Recientemente Requena y cols., describen las características histológicas de este tipo de tumores. En la biopsia cutánea, por tinción con hematoxilina-eosina, se observan células fusiformes distribuídas en dermis que dibujan luces vasculares irregulares. Puede haber extravasación hemática (imagen adjunta). Los restos de hematíes degradados pueden formar los glóbulos hialinos, que son estructuras esféricas, eosinófilas y PAS positivas. No son exclusivos del SK ya que se pueden observar en granulomas piogénicos, tejido de granulación y angiosarcomas. El signo del promontorio también se ha descrito en estos tumores y consiste en luces vasculares que disecan vasos preexistentes. 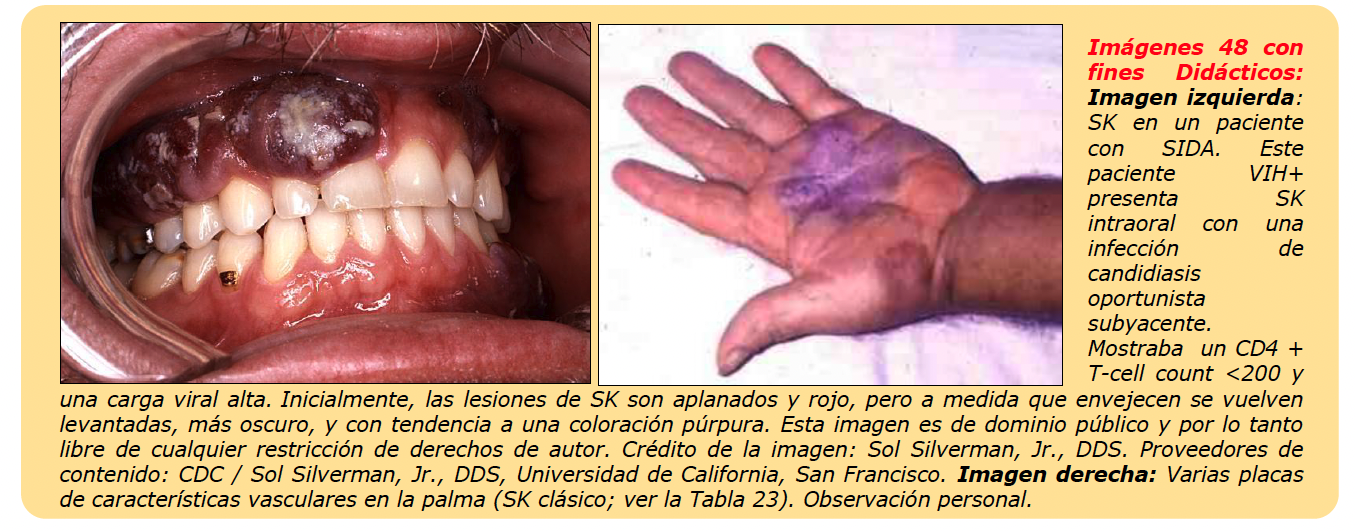
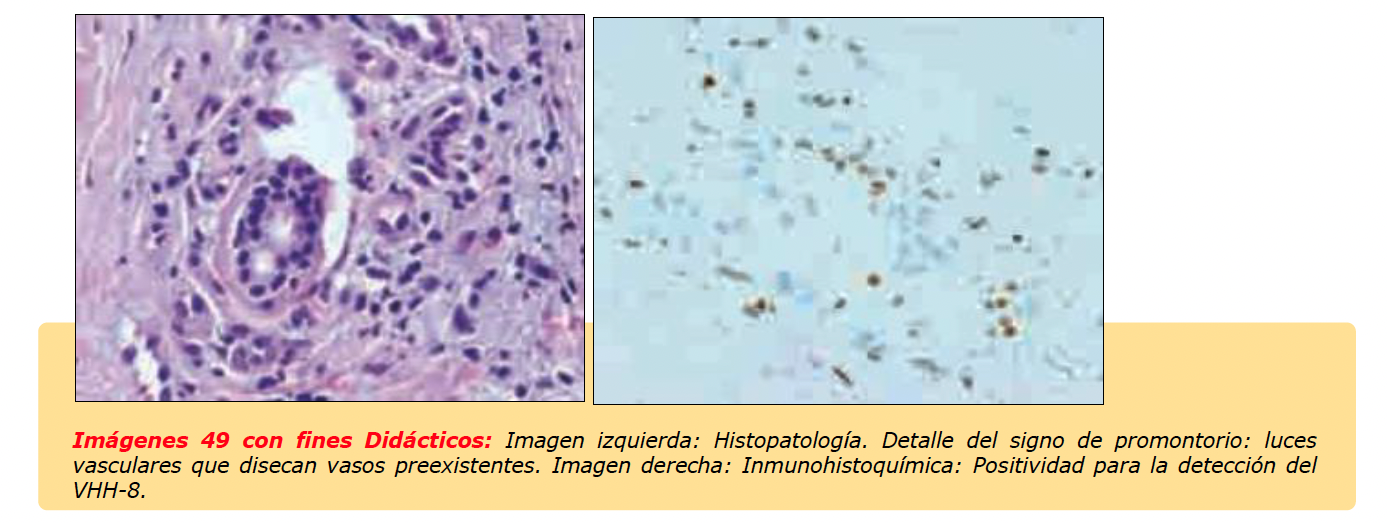
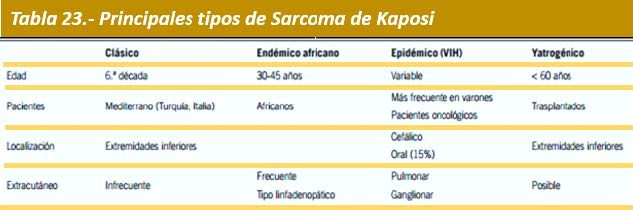
A medida que las lesiones se transforman en placas y nódulos, se produce un aumento de la celularidad fusocelular con luces vasculares irregulares. Puede haber atipias y mitosis, aunque a pesar de ser un tumor maligno no se caracteriza por presentar un índice mitótico muy elevado. Las técnicas de Inmunohistoquimica pueden ayudar en el diagnóstico, especialmente en lesiones incipientes o dudosas. Las luces vasculares son de origen linfático y se marcan con el anticuerpo D2-40 que marca endotelio linfático. Otros marcadores de endotelio vascular, no linfático pueden ser positivos como CD31 y CD34.
El VHH-8 está implicado en su patogenia. Se puede realizar detección del DNA viral por técnicas de reacción en cadena de la polimerasa o bien con anticuerpos monoclonales frente el antígeno nuclear de latencia del VHH-8 (LANA-1) Se ha descrito otras variantes histológicas de sarcoma de Kaposi:
- -Variante anaplásica, poco frecuente y caracterizada por el gran pleomorfismo celular con abundantes mitosis. Se observa en pacientes con sarcoma de Kaposi africano y el asociado a VIH. Es una variante más agresiva con mayor poder metastático.
- -Variante linfangiomatosa, es poco frecuente. Se puede presentar en cualquiera de los cuatro tipos de sarcoma de Kaposi; clásico, endémico, asociado a VIH y el yatrogénico.
- -Variante ampollosa, debido al gran edema en dermis superficial.
- -Variante telangiectásica, sólo existe un caso de un paciente con timoma y miastenia gravis, en tratamiento inmunosupresor durante largo periodo de tiempo. Presentaba lesiones de sarcoma de Kaposi nodular que en la histología mostraba grandes luces vasculares ectásicas.
- -Variante hiperqueratósica o verrucosa, relacionada con el linfedema que se observa en pacientes con infección por VIH. El linfedema crónico induciría cambios de hiperqueratosis y acantosis en la piel afecta. La masa tumoral se puede hallar más profunda en la dermis, haciendo las biopsias tipo “shaving” inadecuadas para el diagnóstico.
- -SK queloidal con tres casos descritos en 1994. En dermis se observa un colágeno denso que puede enmascarar las células fusiformes típicas del sarcoma de Kaposi.
- -SK micronodular, descrito recientemente. Las células fusiformes adquieren una disposición nodular en dermis reticular. Se ha observado en casos de sarcoma de Kaposi clásico y asociados a VIH.
- -Variante tipo granuloma piogénico. Las lesiones nodulares que se traumatizan pueden inflamarse y simular histológicamente un granuloma piogénico. A parte, algunos granulomas piogénicos pueden presentar cambios histológicos que recuerden a un sarcoma de Kaposi.
- -SK equimótico presenta una notable extravasación de hematíes. Se relaciona con casos de sarcoma de kaposi asociado a VIH. Clínicamente se confunden con equimosis o manchas en vino de Oporto.
- -SK intravascular. Se han descrito 6 casos; 4 en pacientes con sarcoma de kaposi clásico y dos en pacientes con sarcoma de kaposi asociado a infección por VIH. Se observa proliferación de células fusiformes en el interior de luces vasculares.
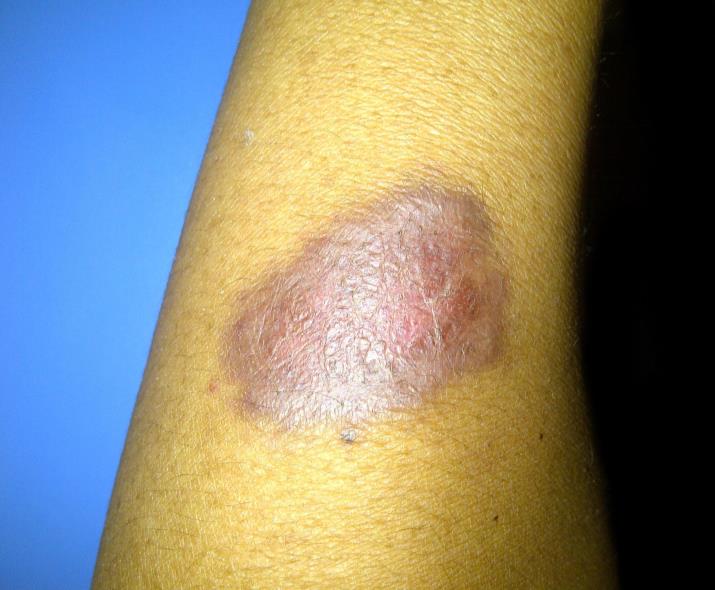
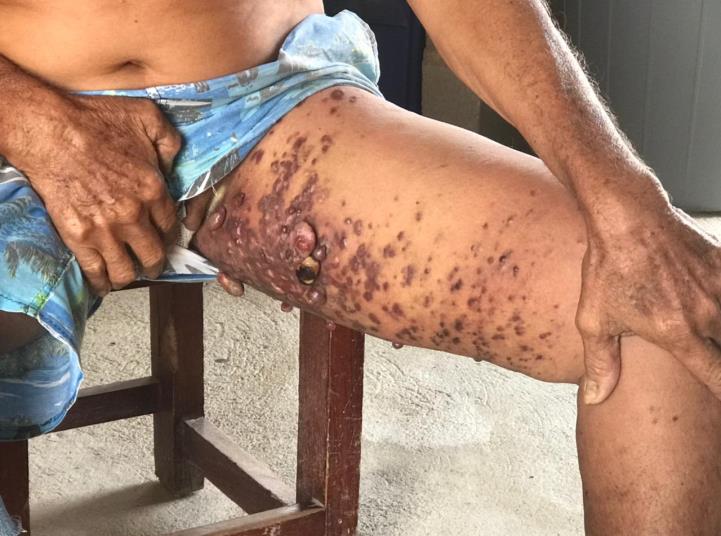
Clínica: Las lesiones se inician en forma de máculas eritemato-violáceas que evolucionan a placas y nódulos. Estos últimos se pueden ulcerar y sangrar. Las lesiones pueden variar desde pequeño tamaño hasta varios centímetros de diámetro. En su evolución pueden permanecer estables durante meses, incluso años o crecer rápidamente y diseminarse.
Se han descrito en la literatura hasta diez variantes diferentes: macular, en placas, en nódulo, linfadenopática, exofítica, infiltrativa, equimótica, telangiectásica, queloidal y cavernosa o linfangiomatosa.
La forma linfadenopática aparece en niños africanos y es letal en una alta proporción de casos. Las formas exofítica e infiltrativa se presentan en adultos africanos. La forma cavernosa o linfangiomatosa se presenta en adultos en forma de linfedema crónico y lesiones en extremidades inferiores en forma de nódulos compresibles que parecen estructuras quísticas rellenas.
En la histología de esta variante cavernosa se observan redes de vasos linfáticos dilatados, irregulares y compresibles. Las células que revisten el endotelio de estos vasos linfáticos son planas y sin atipia citológica. Localizaciones frecuentes de sarcoma de Kaposi son piel, mucosa oral, ganglios. A nivel visceral, los órganos más frecuentemente afectados son pulmón, tracto gastrointestinal, genitales externos, orofaringe, amígdalas, cavidad nasal, hígado, bazo y médula ósea. Se han descrito casos con localizaciones menos frecuentes como hueso, nervios periféricos, laringe, cerebral, ojo y oído, glándulas salivales, corazón, riñón, páncreas.
En general, la afectación gastrointestinal y oral es más frecuente en pacientes con sarcoma de kaposi asociado a VIH. No se realizan endoscopias de rutina a no ser que el paciente refiera semiología intestinal.
En la mayoría de casos, el sarcoma de kaposi sigue un curso crónico, indolente. No obstante, la ausencia de una terapia que erradique al VHH8 hace que no podamos hablar de curación. Con los diferentes tratamientos se intenta mantener la enfermedad estable y evitar la progresión.
Patogenia: En general podemos referir tres causas de SK: el VHH-8, la inmunosupresión y la yatrogenia.
-Virus VHH8: Es un gammaherpes virus, DNA implicado en la patogenia del sarcoma de Kaposi, tanto es así que también recibe el nombre de virus herpes asociado a sarcoma de kaposi. También se ha visto implicado en enfermedad de Castleman, en su variante multicéntrica o plasmoblástica y en el linfoma de cavidades.
Es un virus oncogénico se integra en el DNA celular y tiene diferentes efectos que promueven la producción de tumor.
1. Aumento de la proliferación celular por inhibición de genes que regulan el ciclo celular como p53 y Rb.
2. Promueve la producción de citoquinas pro-angiogénicas como IL6, IL8, TNF beta y VEGF (factor de crecimiento de endotelio vascular). Se ha comprobado la regresión de sarcomas de Kaposi con el uso de fármacos anti-VEGF en modelos murinos.
3. El virus evade el sistema inmune. Las primeras vías del sistema inmune ante una infección vírica son interferón y complemento. El virus inhibe la vía del interferón y con la producción de KCP (proteínas de control de complemento) inhibe el complemento. No obstante, la serología positiva para el VHH-8 no determina por sí sola la aparición de la patología. Se postulaba la posibilidad de transmisión sexual de este virus dado que en los niños no se hallaban anticuerpos frente éste. Emond y cols. realizaron un estudio en París, en el que querían determinar la prevalencia de serologías positivas para VHH8 en pacientes en lista pre-trasplante, cuál era la tasa de seroconversión tras el trasplante y cuál era el riesgo de desarrollo de sarcoma de Kaposi. Observaban una prevalencia de serologías positivas del 2,7% en los pacientes en lista de trasplante, similar a la de la población general de París. Sólo se registro un caso de seroconversión post-trasplante. En países con bajas prevalencias de infección por VHH8, determinar el estado serológico de un paciente pre trasplante no tiene mucho interés, pero esto podría resultar de utilidad en países con alta endemicidad.
El hecho de conocer el estado de portador de VHH8 en un paciente pre trasplante puede ayudar a realizar un diagnóstico precoz en estos pacientes, incluso con signos clínicos incipientes como el edema en extremidades inferiores.
También se puede tener en cuenta a la hora de plantear el tratamiento inmunosupresor en estos pacientes, incluyendo en sus pautas terapéuticas agentes con menor poder carcinogénico como sirolimus.
•Sarcoma de Kaposi yatrogénico: Este tipo de sarcoma de Kaposi se presenta en pacientes con sistema inmune comprometido ya sea por su enfermedad de base o por los tratamientos que reciben. Se han descrito casos en pacientes con enfermedades autoinmunes o inflamatorias que precisan tratamientos inmunosupresores, principalmente corticoides sistémicos. Una de las series más largas publicadas recientemente de sarcoma de kaposi yatrogénico en pacientes trasplantados pertenece al grupo italiano de Piselli y cols. Así pues, este tipo de sarcoma de kaposi yatrogénico, es más frecuente en varones y la edad media de presentación es más joven que en la variante clásica.
La inmunosupresión: Clásicamente se había considerado que los pacientes con trasplante renal tenían un mayor riesgo de padecer sarcoma de Kaposi yatrogénico. Actualmente, se considera que el principal factor de riesgo para el desarrollo de sarcoma de Kaposi yatrogénico es el grado de inmunosupresión y no el tipo de trasplante, aunque sí es cierto que determinados tipos de trasplante precisan de pautas inmunosupresoras más potentes para evitar el rechazo, tal como sucede en el trasplante cardíaco. Se utilizan diversos fármacos para evitar el rechazo de órgano trasplantado: corticoides orales, ciclosporina, tacrolimus, sirolimus.
La ciclosporina tiene un fuerte poder inmunosupresor, pero es bien conocido su riesgo carcinogénico. El sirolimus o rapamicina, es un inhibidor de mTOR. Aunque posee menos poder inmunosupresor que la ciclosporina para evitar el rechazo, se ha visto que ejerce un efecto anti-angiogénico y por ello anti-tumoral. Campistol y cols, han descrito casos de pacientes con regresión del sarcoma de Kaposi yatrogénico tras el cambio de su medicación inmunosupresora por sirolimus. La serie más larga descrita por este grupo de autores, es de 2005 con 7 pacientes trasplantados renales, afectos de SK yatrogénico, todos ellos en extremidades inferiores con regresión del sarcoma en 6 de 7 en 8 meses tras el inicio de sirolimus, dejando una leve atrofia hiperpigmentada.
•Estadiaje
No existe un consenso sobre el estadiaje en el sarcoma de Kaposi.
Se ha propuesto una clasificación del sarcoma de Kaposi en los siguientes estadíos:
– Estadío I o maculopapular: Pequeñas máculas en extremidades inferiores.
– Estadío II o infiltrativo: Placas en extremidades inferiores.
– Estadío III o florido: Múltiples placas angiomatoides y nódulos en extremidades inferiores que se ulceran.
– Estadío IV o diseminado: Las placas y nódulos se extienden más allá de las extremidades inferiores.
Los estadíos I y II se subdividen en:
– Grupo A: progresión lenta.
– Grupo B: progresión rápida, con aumento del número de placas/nódulos o de la extensión que éstos ocupan en 3 meses desde la última exploración.
Los pacientes en estadios I y II suelen presentar menos complicaciones y menor afectación gastrointestinal y visceral; lo contrario que en los pacientes en estadío III y IV.
Los pacientes en estadío IV presentan toda una progresión rápida. Este tipo de estadiaje no se usa ampliamente, pero puede ayudar a predecir la evolución de los pacientes en función de la clínica que presentan.
Tratamiento: Las opciones terapéuticas para el tratamiento del SK son múltiples; cirugía, radioterapia y quimioterapia. El tratamiento en el SK debe ser individualizado. La elección de un tratamiento depende de si se trata de lesiones únicas o enfermedad diseminada, si hay afectación visceral y del estado inmunológico del paciente.
Bibliografía
- KAPOSI M. Idiopathisches multiples Pigmentsarkom der Haut. Arch Dermatol Syph (Prague). 1872;4:265-73.
- Emond JP, Marcelin AG, Dorent R, Milliancourt C, Dupin N, Frances C et al. Kaposi’s sarcoma associated with previous human herpesvirus 8 infection in heart transplant recipients. J Clin Microbiol 2002; 40: 2217-9.
- E. Hernández-Ruiz, A. García-Herrera, J. Ferrando. Sarcoma de Kaposi. Med Cutan Iber Lat Am 2012;40(2):39-48. DOI:10.4464/MD.2012.40.2.5010
- S. Plancoulaine; Gessain (2005). «Aspectos épidémiológicos del herpes humano 8 (HHV-8) et du sarcome de Kaposi». Médecine et Maladies Infectieuses 35 (5): 314-21.
- Piselli P, Busnach G, Citterio F, Frigerio M, Arbustini E, Burra P et al. Risk of Kaposi sarcoma after solid-organ transplantation: multicenter study in 4,767 recipients in Italy, 1970-2006. Transplant Proc 2009; 41: 1227-30
- Campistol JM, Gutiérrez-Dalmau A, Torregrossa JV. Conversion to sirolimus: a successful treatment for posttransplantation Kaposi’s sarcoma. Transplantation 2004; 77: 760-2.
- Toschi E, Sgadari C, Monini P, Barillari G, Bacigalupo I, Palladino C et al. Treatment of Kaposi´s sarcoma: an update. Anti-Cancer Drugs 2002; 13: 977-87.
- Pantanowitz L, Dezube BJ. Kaposi sarcoma in inusual locations. BMC Cancer 2008; 8: 190.
- Gambús G, Bourboulia D, Esteve A, Lahoz R, Rodríguez C, Bolao F et al. Prevalence and distribution of HHV-8 in different subpopulations, with and without HIV infection, in Spain. AIDS 2001; 15: 1167-74.
- Szajerka T, Jablecki J. Kaposi´s sarcoma revisited. AIDS Rev 2007; 9: 230-6.
- Eng W, Cockerell CJ. Histological features of Kaposi sarcoma in a patient receiving highly active antiviral therapy. Am J Dermatopathol 2004; 26: 127-32.
- Requena L, Requena C. Histopathology of the more common viral skin infections. Actas Dermosifiliogr 2010; 101: 201-16.
- Grayson W, Pantanowitz L. Histological variants of cutaneous Kaposi sarcoma. Diagnostic Pathol 2008; 3: 31.
- http://data.unaids.org/pub/report/2010/ecuador_2010_country_progress_report_es.pdf
- JJ Goedert (2000). «La epidemiología de las neoplasias malignas del síndrome de inmunodeficiencia adquirida». Semin Oncol 27 (4): 390 – 401. http://dentistry.ucsf.edu/about-the-school/news-room/press-releases/2014/08/14/sol-silverman-passes-away