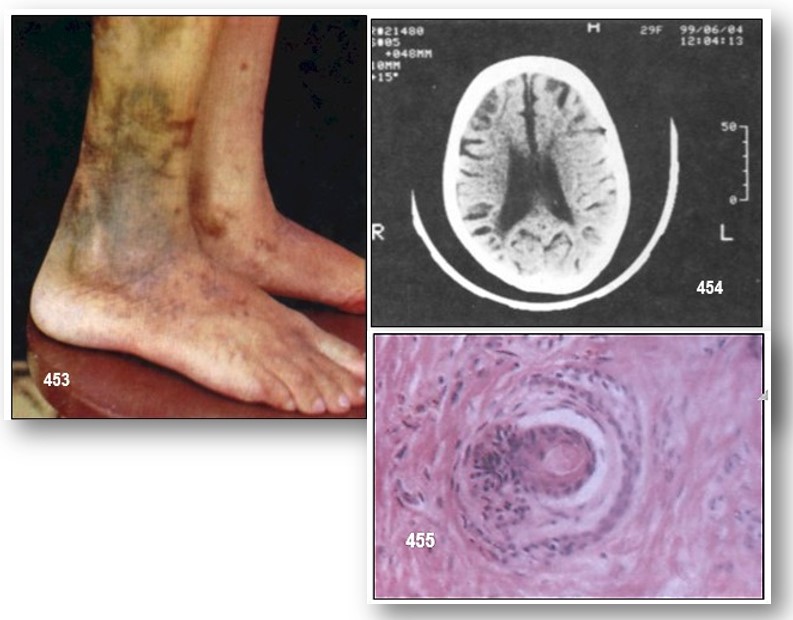
INFORMACIÓN BÁSICA: VASCULITIS: Síndrome antifosfolipídico (SAF): Esta entidad presenta hasta un 40% de los casos manifestaciones cutáneas. El SAF puede definirse como una alteración adquirida y multisistémica caracterizada por un estado de hipercoagulación, la cual se manifiesta como trombosis del sistema venoso, arterial o de ambos sistemas vasculares y actualmente existe información acerca de daño renal ocasionado por los anticuerpos antifosfolipídicos (AAF) al endotelio vascular. El SAF se presenta usualmente en adultos jóvenes, sin embargo se ha descrito en niños y en ancianos, con una prevalencia en la población general del 1 al 5%. No existe un grupo racial predominante, aunque se describe más el lupus eritematoso sistémico (LES) en negros y latinos, y hay que tener en cuenta que muchos casos de SAF corresponden al LES. De hecho, un tercio de pacientes con LES tienen AAF, pero no todos presentan un SAF; el 2% de personas normales tienen AAF detectables y en el 0,2% el título es alto.
Los marcadores serológicos más caracterizados de este síndrome son: los anticuerpos antifosfolipídicos (AAF) que están representados por el anticoagulante lúpico (AL) y los anticuerpos anticardiolipina (AAC).
Sinónimos.- síndrome del anticuerpo antifosfolipídico, síndrome anticardiolipina, trombosis del anticoagulante lúpico, síndrome de Hughes.
Mecanismos patogénicos.- La trombosis venosa y/o arterial, la trombocitopenia y la pérdida fetal han sido asociadas con la presencia de AAF. Una de las claves el rol de los AAF en el mecanismo de la enfermedad, es importante dilucidar si estos son agentes causales, un epifenómeno, una asociación o una consecuencia del daño tisular. Los AAF constituyen un grupo heterogéneo de autoanticuerpos dirigidos a proteínas plasmáticas que se unen a fosfolípidos. Algunos tienen una acción paradójica, in vivo producen trombosis y en vitro actúan como anticoagulantes (anticoagulante del LES). Por otro lado, los AAF activan la cascada de la coagulación y la inflamación. Se ligan a plaquetas en una reacción mediada por la β2 glicoproteína 1 y células endoteliales, activan las células endoteliales e inducen un estado procoagulante. Los anticuerpos AL son importantes porque correlacionan fuertemente con las complicaciones trombóticas y obstétricas del síndrome.
En relación a hallazgos de laboratorio que puedan explicar las manifestaciones clínicas se tienen los siguientes hechos:
- – La inmunización pasiva de ratones con anticuerpos murinos reproducen la pérdida fetal observada en humanos, así como inmunoglobulinas humanas purificadas inducen trombos en venas injuriadas de ratones.
- – Los AAF pueden causar directamente trombosis.
Muchos hallazgos pueden explicar esta hipótesis:
- – Daño y activación del endotelio
- – Interferencia con la producción y liberación de prostaciclinas de las células endoteliales
- – Activación de las plaquetas
- – Interferencia con las proteínas “C” y “S”
- – Inhibición del fosfolípido placentario anticoagulante, proteína 1
- – Interferencia con la actividad de la antitrombina III
- – Falla del sistema fibrinolítico
- – Beta 2-GPI (Apolipoproteína H), otro anticuerpo presente en SAF, alcanza a unirse con los anticuerpos antifosfolípidos o fosfolípidos y pueden ser requeridos para el desarrollo de este síndrome.
Es necesario recordar el rol del endotelio en el tono vascular, en los mecanismos de trombosis -fibrinólisis y en los procesos inflamatorios, para entender la fisiopatología del SAF. La actividad anticoagulante ocurre a través de la activación e interacción de estos tres mecanismos, la antitrombina III, las proteínas “C” y “S” y el sistema fibrinolítico.
Manifestaciones Clínica.-Las manifestaciones cutáneas en el SAF son muy diversas, como se señaló anteriormente se presentan en un 40% de los casos, y pueden ser la primera manifestación clínica de una enfermedad subyacente, por lo que es conveniente estar familiarizado con estos hallazgos que permitirán plantear esta posibilidad diagnóstica.
El Livedo reticularis (imagen 51) es el signo más caracterizado del SAF, es posible que se deba al estasis circulatorio ocasionado por la oclusión vascular. Hay asociación entre livedo reticularis y acrocianosis en pacientes con SAF primario. La Tabla 30 resume las diferentes manifestaciones clínicas del SAF.
Otras manifestaciones cutáneas asociadas al SAF: Acrocianosis, Ulceración, Necrosis, Fenómeno de Raynaud, Capilaritis, Maculas purpúricas/cianóticas, Nódulos, Isquemia digital/gangrena, Síndrome del Dedo azul, Tromboflebitis, Hemorragias, Atrofia blanca.
El Livedo reticularis (imagen 453) es el signo más caracterizado del SAF, es posible que se deba al estasis circulatorio ocasionado por la oclusión vascular. Hay asociación entre livedo reticularis y acrocianosis en pacientes con SAF primario.
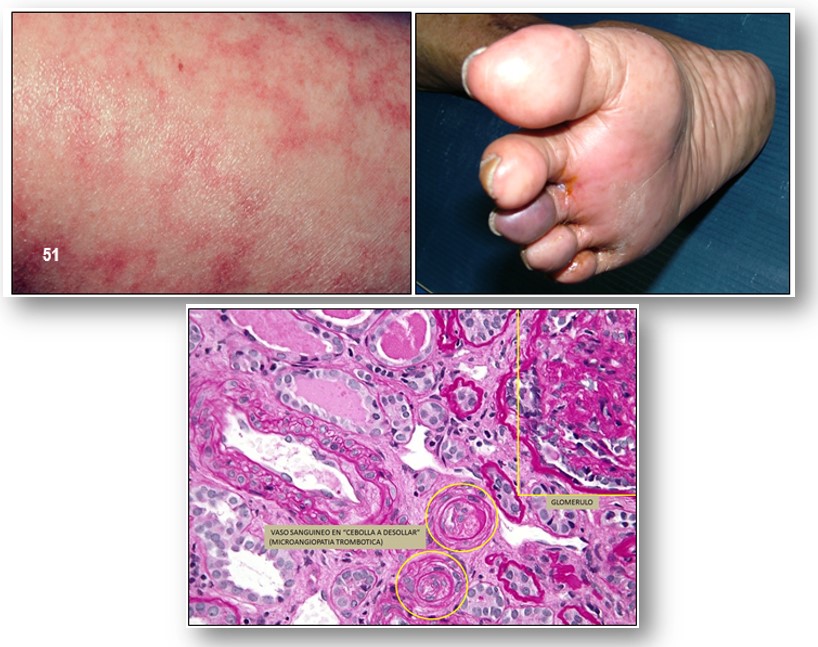
El Livedo reticularis (imagen 51) es el signo más caracterizado del SAF, es posible que se deba al estasis circulatorio ocasionado por la oclusión vascular. Hay asociación entre livedo reticularis y acrocianosis en pacientes con SAF primario.
Otras manifestaciones cutáneas asociadas al SAF: Acrocianosis, Ulceración, Necrosis, Fenómeno de Raynaud, Capilaritis, Maculas purpúricas/cianóticas, Nódulos, Isquemia digital/gangrena, Síndrome del dedo azul, Tromboflebitis, Hemorragias, Atrofia blanca.
Clínicamente el livedo reticularis (imágenes) se describe como un patrón reticulado de la piel, frecuentemente encontrado en el tronco y extremidades, la estasis vascular en capilares y vénulas superficiales dilatadas le confieren ese matiz purpúrico, se ha descrito en diferentes enfermedades tales como las del tejido conectivo, como el LES, púrpura trombocitopénica idiopática, enfermedad vascular ateromatosa, en el síndrome de Sneddon, que constituirán los diagnósticos diferenciales más importantes. La trombosis puede ocurrir en cualquier lugar del sistema venoso o arterial, lo más frecuentemente reportados son el compromiso de las venas superficiales y profundas de las piernas, la vena renal, las venas hepáticas y la vena porta y la vena cava inferior.
Es más frecuente en el sistema arterial la oclusión de las arterias cerebrales, arteria de la retina, las coronarias y la trombosis de arterias periféricas que puede resultar en gangrena de las extremidades. En la placenta se ha descrito trombosis vascular que ocasiona infarto placentario y pérdida fetal. Se han encontrado mayor asociación entre trombosis y trombocitopenia, en pacientes con niveles elevados de ACL y livedo reticularis en comparación con otros pacientes, mientras que McHugh NJ y col. encuentran asociación entre livedo reticularis e incremento de IgG ACL, enfermedad cerebro-vascular y renal.
Las ulceras cutáneas, algunas semejantes al pioderma gangrenoso, han sido el signo de presentación del SAF, la ubicación más frecuente es en los miembros inferiores que en ocasiones pueden ser lesiones profundas y dolorosas. Otra forma de presentación del SAF puede ser la necrosis cutánea, el término púrpura necrotizante ha sido aplicado a una forma de necrosis que se presenta en este desorden, siendo las zonas de más frecuente ubicación las piernas, la cara, las orejas y en ocasiones adquieren formas generalizadas. Isquemia distal y la gangrena digital es una consecuencia de la oclusión arteriolar sostenida.
Por otro lado, el SAF se puede manifestar de múltiples formas (excluyendo en esta redacción, las manifestaciones cutáneas, ya descritas) que incluyen: trombosis venosas y arteriales, abortos espontáneos recurrentes y trombocitopenia. Otros posibles hechos son: cefaleas migrañosas, disfunción neurológica, enfermedad renal, hipertensión pulmonar, necrosis avascular e insuficiencia adrenal. A continuación detallo el espectro clínico del SAF, a pesar de que la mayoría de los casos son asintomáticos:
– Trombosis: La trombosis venosa es más frecuente que la arterial, principalmente la de la pantorrilla. Otras posibles localizaciones son renales, hepáticas y retinianas. Las trombosis arteriales más comunes son las cerebrales, aunque también se puede presentar como trombosis de las arterias coronarias, renales, mesentérica o como oclusiones de bypass. La trombosis venosa y sus complicaciones son más frecuentes que la trombosis arterial. En una cohorte de 1000 el primer síntoma fue trombosis venosa profunda de la pierna en 32% y embolismo pulmonar en 14%. Otros vasos tales como venas renal, hepática, subclavia y retiniana, senos cerebrales y vena cava son afectados con mayor frecuencia que en trombosis no relacionada con SAF. Las complicaciones trombóticas arteriales son ataque cerebral y ataque isquémico transitorio, que son la manifestación clínica inicial en 13% y 7% de los pacientes, respectivamente.
Las recurrencias de las trombosis son frecuentes (70% las venosas y 90% las arteriales).
– Enfermedad cerebrovascular: Ocurren accidentes isquémicos transitorios (simples o múltiples) y/o accidentes cerebrovasculares, y a menudo recurren, lo que origina demencia o gran variedad de déficits neurológicos temporales o permanentes, como la mielopatía transversa, epilepsia, corea, demencia multiinfarto, síndrome de Guillain Barré, amnesia transitoria global, enfermedad de la motoneurona, depresión y pseudotumor cerebral. Algunos son secundarios a trombosis arteriales cerebrales y otros tienen causa embolígena (endocarditis de Libman-Sacks); pueden llevar a la confusión con psicosis esteroidea, meningitis aséptica y esclerosis múltiple. Debe sospecharse en pacientes jóvenes sin factores de riesgo. Véase la Tabla 2.
Manifestaciones oftalmológicas: En algunos casos, los pacientes pueden presentar inicialmente con sólo hallazgos oculares. La detección temprana y el tratamiento pueden prevenir una mayor morbilidad sistémica y la mortalidad.
El trabajo en marcha está especialmente justificado en pacientes jóvenes sin factores conocidos de riesgo sistémico que presentan enfermedad vascular oclusiva o uveítis asociada con vasculitis de etiología desconocida. Los pacientes a menudo se presentan con síntomas visuales incluyendo visión borrosa monocular o binocular de la visión, amaurosis fugaz, escotoma transitorio y defectos del campo visual. Otros síntomas citados en la literatura son los síntomas de ojo seco, enrojecimiento y dolor. Es importante destacar que, binocular amaurosis fugaz por lo general representa la isquemia del SNC.
– Trombosis venosa: Tiene correlación con los niveles de AAC. Los pacientes con LES y AAC también tienen una alta incidencia de trombosis.
– Enfermedad pulmonar: Se puede desarrollar un amplio abanico de enfermedades pulmonares. Las más comunes son el embolismo pulmonar e infarto (un tercio) y la hipertensión pulmonar tromboembólica y no tromboembólica; también se dan casos de trombosis microvascular pulmonar, capilaritis pulmonar y hemorragia alveolar.
Se ha descrito el llamado síndrome postparto, que consiste en fiebre, dolor pleurítico, disnea e infiltrados parcheados.
– Enfermedad cardiovascular: Engrosamiento valvular y desarrollo de vegetaciones (válvula mitral y aórtica, tipo endocarditis): conduce a insuficiencia valvular, embolias cerebrales y cuadros sugestivos de endocarditis infecciosa (fiebre, hemorragias subungueales, hemocultivos negativos).
- Trombos intracavitarios.
- Cardiomiopatía (trombosis en la microcirculación miocárdica).
- Prematura reestenosis de bypass. Fallo de angioplastia.
- Enfermedad periférica vascular.
A pesar de todo ello, existe controversia sobre la asociación entre el SAF y un incremento de la incidencia de infarto de miocardio.
– Manifestaciones hematológicas: Trombocitopenia y púrpura trombótica trombocitopénica (microangiopatía trombótica). A mayor número de AAC IgG, mayor trombopenia y mayor riesgo de trombosis.
– Episodios de sangrado: Debe sospecharse la presencia de anticuerpos protrombínicos cuando un paciente con un SAF conocido desarrolla manifestaciones de sangrado antes que trombosis.
– Enfermedad renal: No está clara su fisiopatología. Parece ser consecuencia de trombosis y estenosis de las arterias renales y depósitos de fibrina en los glomérulos. La clínica varía desde:
- Proteinuria inferior a 2 g/día, con función renal normal.
- Fallo subagudo con proteinuria y alteración del sedimento.
- Hipertensión grave y dolor en flanco, uni o bilateral, en pacientes con infartos renales.
– Glándulas suprarrenales: Enfermedad de Addison secundaria a trombosis de las arterias suprarrenales. Hipopituitarismo.
– Enfermedad gastrointestinal: Sangrado, dolor abdominal, abdomen agudo, necrosis esofágica con perforación o ulceración gástrica gigante o atípica duodenal, todo ello secundario a isquemia a la altura de esófago, estómago, duodeno, íleo o colon. Otras: Síndrome de Budd-Chiaria. Necrosis hepática. Isquemia intestinal.
– Manifestaciones cutáneas: Ya descritas en parte en líneas anteriores, y entre ellas la más representativa es el livedo reticularis: otras como la enfermedad de Degos (papulosis maligna atrófica), necrosis cutánea e infartos, hemorragias subungueales, tromboflebitis, gangrena digital, ulceraciones en la piel y lesiones parecidas a vasculitis (nódulos y máculas).
– Otras enfermedades reumatológicas: Se han visto AAF en el 20% de la Polimialgia reumática y arteritis de células gigantes, aunque su presencia en estos pacientes no se asocia con un incremento del riesgo de trombosis.
– Oseas: Necrosis ósea avascular.
– Pérdidas fetales recurrentes: Habitualmente ocurren a partir de la décima semana de gestación, aunque estudios más recientes han extendido los efectos deletéreos de los AAF a mujeres con pérdidas recurrentes preembriónicas y embriónicas. Hasta en un 10-20% de ellas aparecen AAF sin otra causa médica que las justifiquen; no se conocen con exactitud los mecanismos patogénicos:
– Trombosis progresiva de la microcirculación de la placenta que podría llevar a insuficiencia placentaria, aunque no se han hallado áreas de infartos en todas las placentas.
– Los AAF pueden también dañar la invasión trofoblástica y la producción hormonal, lo que da lugar a pérdidas preembrióticas, embrióticas y fetales, así como a insuficiencia uteroplacentaria.
– El feto sólo presenta un retraso del crecimiento.
– La preeclampsia es frecuente en gestantes con AAF.
– Trombocitopenia: Es relativamente común en pacientes con AAF, aunque no tan grave como para causar una hemorragia. El número de plaquetas suele permanecer estable durante años, pero en algún momento se produce un descenso que puede ser importante.
Algunos pacientes con SAF pueden presentar sólo trombocitopenia y más tarde desarrollar trombosis o pérdidas fetales.
Determinados pacientes también desarrollan anemia hemolítica con prueba de Coombs directa positiva (síndrome de Evans/Este síndrome es una entidad clínica autoinmune (rara) se manifiesta por la presencia de trombocitopenia y anemia hemolítica, las cuales pueden variar en el tiempo de aparición, el curso o su duración).
Tipos de trombosis en pacientes con anticuerpos antifosfolípidos:
– Tipo I: Trombosis venosa profunda en extremidades superiores e inferiores. Trombosis en la vena cava inferior, hepática portal y renal.
– Tipo ll: Trombosis arterial incluyendo arterias coronarias, arterias periféricas y aorta.
– Tipo lll: Trombosis vascular en la retina o el cerebro.
– Tipo lV: Combinación de los tipos anteriores.
Factores de riesgo: Los factores de riesgo para el desarrollo de un SAF incluyen:
- – SAF primario
- – Marcador genético HLA-DR7
- – SAF secundario
- -LES u otro desorden autoinmune marcadores genéticos: HLA-B8, HLA-DR2, HLA-DR3
Consideraciones diagnósticas: Se debe sospechar de un SAF en caso de un evento clínico marcador tal como una trombosis venosa o arterial sin causa aparente, trombocitopenia y en caso de pérdidas fetales recurrentes. El diagnóstico definitivo se hace por laboratorio. Las pruebas de laboratorio para el SAF se hacen en base a dos ensayos, el ensayo para demostrar la presencia de AL y el ensayo de AAC que se hace por ELISA.
La trombofilia de origen genético es parte del diagnóstico diferencial en caso de SAF, y puede coexistir en algunos pacientes con SAF. La presencia de una trombofilia genética puede determinar la necesidad de terapia anticoagulante. Un panel para diferenciar trombofilia genética podría consistir en:
– Estudios para determinar la variante Factor V Leiden y mutaciones de la protrombina, niveles de factor VIII, mutaciones de la MTHFR (hiperhomocisteinemia).
– Niveles de proteína C, proteína S libre y total, antitrombina, plasminógeno, activador tisular del plasminógeno, y activador inhibidor del plasminógeno-1 (PAI-1)
La búsqueda de anticuerpos dirigidos contra cada uno de los posibles objetivos de los AAF (por ejemplo anticuerpos anti-β2 glicoproteína 1 y anti fosfatidilserina) se encuentra actualmente en debate, ya que de momento el ensayo para anticuerpos anticardiolipinas parece ser más sensible y específico para el diagnóstico de SAF, incluso a pesar de que las cardiolipinas no son consideradas un objetivo de los AAF in vivo.
Diagnostico específico: Un reciente consenso ha simplificado los criterios para el diagnóstico del SAF: presencia de al menos uno de los criterios clínicos y al menos uno de los criterios de laboratorio.
El diagnóstico de SAF requiere tanto de evidencia clínica (eventos clínicos documentados tales como trombosis vascular o problemas obstétricos), como de la presencia confirmada de AAF en ensayos repetidos. El criterio de clasificación de Sapporo para el SAF (1998, publicado en 1999), fue reemplazado luego por el criterio de Sydney en 2006.
De acuerdo al criterio de clasificación más reciente, un diagnóstico de SAF requiere una manifestación clínica y una prueba de laboratorio.
Criterios clínicos:
Manifestaciones clínicas:
Un episodio documentado de trombosis arterial, venosa o de pequeños vasos dentro de cualquier tejido u órgano, que no sea trombosis venosa superficial en ningún tejido u órgano, y validada por un criterio objetivo sin evidencia significativa de inflamación (vasculitis) en el vaso sanguíneo y/o:
Complicaciones del embarazo:
– 1 o más muertes fetales inexplicables de un feto morfológicamente normal de al menos 10 semanas de gestación (documentado por medio de ultrasonografía o examen directo), y/o 3 o más abortos espontáneos consecutivos antes de las 10 semanas de gestación, habiendo descartado anormalidades anatómicas u hormonales de la madre y anormalidades cromosomales tanto maternas como paternas. O al menos 1 o más nacimientos prematuro de neonatos morfológicamente normal antes de las 34 semanas de gestación debido a eclampsia o preeclampsia severa de acuerdo a sus definiciones estándar, o evidencias reconocibles de insuficiencia placentaria.
– 3 o más abortos espontáneos consecutivos inexplicados antes de la décima semana de gestación.
Parámetros de laboratorio: El diagnóstico del SAF se basa en los criterios de clasificación de Sidney (2006), donde la positividad de las pruebas de laboratorio (anticuerpos anticardiolipina [AAC], anti-β2-glicoproteína 1 o anticoagulante lúpico [AL]) supone un requisito necesario. Sin embargo, no es infrecuente encontrar pacientes con clínica muy sugestiva del SAF y ausencia de estos anticuerpos.

Pueden encontrarse los patrones siguientes: Trombocitopenia moderada, AL positivo y moderados o elevados títulos de AAC IgG en trombosis venosa e IgM en trombosis arterial, que en el contexto de manifestaciones clínicas de trombosis permite el diagnóstico. La demostración de la presencia de AAC forma uno de los criterios diagnósticos del SAF. Los AAF se dividen para su estudio e interpretación en:
– Anticuerpos Anticardiolipinas (AAC): de los tipos IgG o IgM presentes en niveles moderados o altos en dos o más ocasiones y con al menos 12 semanas de intervalo, por ELISA estandarizado para medir AAC dependiente de anti B2-glicoproteina.
– AAC-IgG: título medio (20-80) o alto (superior a 80).
– AAC-IgM: título medio (20-50) o alto (superior a 50).
– Anticuerpos anti-β2 glicoproteína 1, IgG y/o IgM medida por un ensayo ELISA estandarizado en 2 o más ocasiones, con no menos de 12 semanas de separación, por ELISA estandarizado; a títulos medios o elevados (> al percentilo) y/o
– Anticuerpos anticoagulante lúpico (AAL): detectados en sangre en dos o más ocasiones con al menos 12 semanas de diferencia, de acuerdo a las guías de la Sociedad Internacional en Trombosis y Hemostasia.
Existen 3 entidades SAF distintivas: el SAF primario (en ausencia de cualquier comorbilidad), el SAF secundario (cuando hay alguna condición autoinmune preexistentes, más frecuentemente el LES), y el SAF catastrófico (cuando aparece falla multiorgánica simultánea con oclusión de pequeños vasos; véase más adelante).
De acuerdo a las declaraciones del consenso de Sidney, es conveniente, para propósitos de investigación, clasificar al SAF en una de las siguientes categorías:
- I: más de un criterio de laboratorio presentes en cualquier combinación;
- IIa: presencia sólo de AL
- IIb: presencia sólo de AAC IgG y/o IgM a títulos medios o altos
- IIc: presencia sólo de anti-β2 glicoproteína I IgG y/o IgM en títulos mayores al percentilo 99.
La Declaración de Consenso Internacional se utiliza comúnmente para el diagnóstico de SAF catastrófico. Basado en estas declaraciones, el diagnóstico definitivo de SAFLC requiere:
- a) Trombosis vascular en tres o más órganos o tejidos y
- b) Desarrollo de manifestaciones secundarias simultáneamente o antes de la semana ‘y
- c) Evidencia de trombosis de pequeños vasos en al menos un órgano o tejido y
- d) Confirmación de laboratorio para la presencia de AAF.
Algunos ensayos serológicos para sífilis pueden dar resultados positivos en algunos pacientes con AAF positivos (los AAF se unen inespecíficamente a los lípidos presentes en el ensayo y entregan un falso positivo) aunque los test más específicos para sífilis que utilizan antígenos recombinantes darán un resultado negativo.
El diagnóstico de SAF primario o secundario debe hacerse buscando la posible existencia de otra enfermedad autoinmune asociada. En el secundario es más frecuente la presencia de lesiones valvulares cardiacas, anemia hemolítica, niveles de C4 disminuidos y neutropenia.
No es infrecuente que la primera manifestación del LES sea un SAF. Por ello se recomienda un tiempo de observación de al menos 5 años antes de diagnosticar a un paciente de SAF primario.
Aunque los AAF también se presentan en asociación con otras patologías (infecciones, cáncer, uso de drogas, hemodiálisis), son anticuerpos IgM normalmente en niveles bajos y no se asocian con fenómenos trombóticos.
Las pruebas serológicas deben permanecer positivas>12 semanas (hasta 5 años). Periódicamente se realizan reuniones de consenso para unificar criterios de diagnóstico y tratamiento en el SAF. El SAF puede clasificarse como primario o idiopático cuando no se demuestra una causa subyacente y secundario a múltiples causas, de las cuales la más importante es el LES en el grupo de enfermedades inmunológicas. También una asociación importante la constituye la púrpura trombocitopénica autoinmune. Entre los tumores destaca como manifestación paraneoplásica el tumor ovárico; el SIDA; entre las causas medicamentosas está: procainamida, clorpromazina e hidralazina; las causas de SAF secundario son numerosas.
Anticuerpos detectados en el SAF: EL SAF es la causa más común de trombofilia adquirida, afortunadamente rara vez puede haber un curso catastrófico con daño multiorgánico, síndrome de oclusión vascular catastrófico; si ocurriera los pacientes presentan tromboembolismo masivo, cursando con insuficiencia respiratoria, enzimas hepáticas elevadas, daño renal, insuficiencia adrenal e infartos cutáneos múltiples entre las causas más relevantes. El fallo multisistémico (fallo de múltiples órganos), aunque raro, puede ser súbito debido a trombosis generalizada; en este caso se suele utilizar el término SAF catastrófico, y presenta un alto riesgo de vida.
Los AAF también conocidos como AAF o aPL por sus siglas en castellano y en inglés respectivamente, son un grupo heterogéneo de autoanticuerpos tipo IgG, IgM e IgA dirigidos contra diferentes tipos de fosfolípidos y proteínas de unión a fosfolípidos. Estos anticuerpos suelen dividirse para su estudio en anticuerpos anticardiolipinas y anticoagulante lúpico. A continuación, describiré cada uno de ellos.
Los AAF suelen aparecer en varias patologías y situaciones clínicas tales como:
-Enfermedades autoinmunes: –
- – LES.
- – Artritis reumatoide.
- – Enfermedad mixta del tejido conectivo
- – Vasculitis sistémica
- – ESP
- – Dermatopolimiositis
- – Diabetes
- – Lupus discoide
- – Síndrome de Behçet
- – Poliarteritis nodosa
- – Purpura trombocitopénica Idiopática
- – Miastenia gravis
- – Hepatitis crónica activa
- – Enfermedad de Crohn
- – Tiroiditis autoinmune
- – Espondilitis anquilosante
- – Enfermedad de Takayasu.
– Enfermedades hematológicas: –
- – Mielofibrosis
- – Policitemia
- – Anemia perniciosa
- – Paraproteinemias
- – Purpura trombótica trombocitopénica
- – Enfermedad de Von Willebrand.
– Enfermedades neurológicas:
- – Síndrome de Snnedon
- – Miastenia gravis
- – Esclerosis múltiple
- – Migraña.
– Exposición a fármacos:
- – Clopromacina. -Fenotiacinas.
- – Procainamida.
- – Antibióticos.
- – Fenitoína
- – Alfa interferón
- – Hidralazina
- – Clozapina
- – Anticonceptivos orales
- – Quinidina.
- – Infecciones: –
- – Virales, incluido el SIDA.
- – Bacterianas.
- – Micóticas.
- – Sífilis
- – TB
- – Micoplasmas
- – Varicela
- – Parvovirus
- – Paperas
- – Pneumocitys jiroveci
- – Sepsis
- – Lepra
- – Malaria
- – Enfermedad de Lyme
- – Hepatitis A
- – Adenovirus
- – Sarampión
- – Endocarditis
- – Mononucleosis infecciosa.
– Neoplasias:
Tumores sólidos
- Leucemias
- Linfoma de Hodgkin
- Mieloma múltiple
- Micosis fungoide
- Desordenes linfoproliferativos
Individuos aparentemente sanos.
– Anticuerpos anticardiolipinas (AAC):
Estos anticuerpos pueden ser detectados utilizando un inmunoensayo de tipo ELISA que busca la presencia de anticuerpos anti β2-glicoproteína 1 dependientes de anticardiolipinas.
También se puede observar en pacientes con diagnóstico positivo trombocitopenia y anticuerpos anti β2-glicoproteína 1 (no dependiente de cardiolipinas) y anticuerpos anti fosfatidilserina.
– Anticuerpos anti-b2-glucoproteína I: Los anticuerpos anti-b2GPI son inmunoglobulinas que reconocen a esta proteína en presencia de fosfolípidos aniónicos o de una superficie oxidada como el plástico de las placas de ELISA sujetas a irradiación.
Diferentes estudios han relacionado la detección de anti–b2GPI de isotipos IgG e IgM con el riesgo de presentar eventos trombóticos. Su detección puede ser de utilidad en aquellos pacientes que presentan manifestaciones clínicas de SAF, en los cuales las determinaciones de AAC y AL han sido varias veces negativas.
– Anticuerpos antiprotrombina: Otro grupo de autoanticuerpos con actividad AL son los anticuerpos antiprotrombina que se encuentran en un tercio de los pacientes con SAF. Para su detección se utiliza ELISA. Su presencia ha sido asociada a manifestaciones trombóticas en diferentes estudios. Debido a que los mecanismos protrombóticos son multifactoriales y no están de todo dilucidados, la investigación sobre la utilidad clínica de estos autoanticuerpos se sigue desarrollando.
Síndrome antifosfolípido seronegativo: En la práctica clínica no es infrecuente encontrar pacientes con manifestaciones clínicas sugestivas de un SAF que son persistentemente negativos para las pruebas de laboratorio que detectan anticardiolipina (ACL), anticoagulante lúpico (AL) y anti- _2-glicoproteína (GP) 1. Para estos casos se ha acuñado el término SAF seronegativo (SAF-SN). En este sentido, aunque el diagnóstico de SAF se basa en la detección de estos anticuerpos, se han descrito otros anti-cuerpos en pacientes con SAF dirigidos contra diferentes fosfolípidos o cofactores de proteínas, tales como protrombina, fosfatidiletanolamina, anexina V o el complejo vimentina/cardiolipina. Sin embargo, el principal inconveniente es que no forman parte de las pruebas de cribado actuales debido a la ausencia de técnicas de laboratorio estandarizadas para medir estos anticuerpos.
Desde la descripción del SAF-SN, las referencias al mismo se basan en la publicación de casos aislados. Sin embargo, recientemente se ha publicado la experiencia de una serie de 67 pacientes con criterios clínicos de SAF y negatividad persistente de los anticuerpos antifosfolípido (AAF). Estos pacientes reunían además de un criterio clínico mayor como trombosis arterial o venosa o morbilidad obstétrica, 2 o más criterios no incluidos en los criterios de clasificación de Sidney, pero que se acepta se asocian o forman parte del síndrome: livedo reticularis, Raynaud, manifestaciones neurológicas (migraña, disfunción cognitiva, convulsiones, corea, lesiones en sistema nervioso central [SNC] similares a la esclerosis múltiple, lesiones hiperintensas en sustancia blanca del SNC en la resonancia magnética [RM]), enfermedad cardíaca valvular, morbilidad obstétrica (1-2 abortos < 10 semanas) o trombocitopenia. En este estudio se incluyeron además 87 pacientes con diagnóstico de SAF basado en los criterios de Sidney (SAF seropositivo [SAF-SP]). La prevalencia de las manifestaciones trombóticas y obstétricas fue similar en ambos grupos, incluida la recurrencia de los eventos vasculares en pacientes en quienes se suspendió la anticoagulación o los niveles de INR (Internacional Normalized Ratio), no se mantuvieron en rango terapéutico. Se observó una tasa inferior de embarazos con éxito (recién nacidos vivos/número de embarazos) en el grupo SAF-SN (38% vs 50%; p = 0,03), lo que pudo estar relacionado con el hecho de que el SAF-SN es una entidad poco reconocida, y por tanto estas pacientes no habrían recibido el mismo tratamiento durante el embarazo en relación a las pacientes con SAF-SP.
Otros autoanticuerpos: Se han detectado diferentes autoanticuerpos en pacientes con SAF como son los antianexina V, anti-proteína C, anti-proteína S, anti-trombomodulina, anti-LDL oxidada (que podrían estar relacionados con la formación de placas de ateroma), antiplaquetarios, antieritrocitarios, anticélula endotelial, antinucleares y antimitocondriales. Estos autoanticuerpos no se utilizan en la práctica médica común (con excepción de los antinucleares, que pueden ayudar a diferenciar un SAF primario de un síndrome asociado a LES) y su papel patogénico en el SAF se encuentra en fase de investigación.
No se observaron diferencias en los factores de riesgo vascular protrombótico, y los pacientes con eventos vasculares estaban recibiendo tratamiento anticoagulante y otros fármacos concomitantes en similar proporción.
Un análisis posterior de los pacientes de este estudio ha mostrado una sensibilidad diagnóstica en el grupo SAF-SN del 23,5% cuando se determinaron las siguientes pruebas no estándar de laboratorio: IgA anti-2-GP 1 e IgG e IgM antifosfatidilserina-protrombina y antifosfatidiletanolamina. Estos resultados sugieren que se debe contemplar la posibilidad de la presencia de un SAF cuando existen datos clínicos que apoyan este diagnóstico, a pesar de la negatividad de los AAF incluidos en los criterios de clasificación del síndrome vigente. El seguimiento de estos pacientes y el adecuado tratamiento antitrombótico pueden prevenir la recurrencia de las trombosis y mejorar el pronóstico materno-fetal.
Tratamiento: En relación con el tratamiento antitrombótico, un estudio reciente ha señalado la seguridad y eficacia del uso de heparinas de bajo peso molecular (fraxiparine, p. ej,) a largo plazo en pacientes con SAF no subsidiarios de tratamiento con dicumarínicos, hay otros que desdicen de estos hallazgos, como veremos más adelante. Por otro lado, existe un subgrupo de pacientes con SAF y pérdidas fetales recurrentes, cuyo pronóstico materno-fetal puede verse mejorado con la administración de bajas dosis de esteroides durante el primer trimestre de gestación.
A pesar de estas consideraciones no existe consenso para el tratamiento, sin embargo, se indica anticoagulación prolongada y AAS en dosis bajas, la anticoagulación profiláctica no se recomienda en pacientes con AAF presentes si no hay historia de trombosis vasculares. Si hubiera historia de trombosis venosa, embolismo pulmonar, se debe anticoagular de manera prolongada manteniendo un índice internacional normalizado (INR) prolongado. La warfarina es el tratamiento de elección para los pacientes con trombosis, algunos autores sugieren añadir AAS; algunos pacientes presentan recurrencia de trombosis cuando se interrumpe el tratamiento de anticoagulación. El tiempo promedio de tratamiento es de 6 meses, sin embargo, ante los casos de recurrencia se hará anticoagulación de por vida.
Aunque se ha observado que los tratamientos inmunosupresores con corticosteroides, los pulsos con ciclofosfamida, plasmaféresis, gamma globulina humana IV, pueden reducir los niveles circulantes de AAF hay un fenómeno de rebote, por lo tanto, no están generalmente indicados. No hay ensayos clínicos controlados en el tratamiento y prevención del SAF igualmente no hay consenso en cuanto a la duración de la anticoagulación.
Recomendaciones de tratamiento antitrombótico en el síndrome antifosfolípido: Consenso de Galvestone (2010). El manejo de la trombosis en los pacientes con SAF continúa siendo un tema controvertido. Es relevante el hecho de que este síndrome supone una trombofilia adquirida que afecta a un 20% de los pacientes jóvenes con tromboembolismo venoso o con ictus, y estudios observacionales indican que existe una elevada tasa de recurrencia en pacientes con SAF en quienes se suspende el tratamiento antitrombótico. Sin embargo, es bien conocido que la anticoagulación a largo plazo representa un riesgo real de sangrado potencialmente grave. Además, se plantea el dilema acerca de la necesidad de tromboprofilaxis primaria en sujetos portadores de AAF. Con el propósito de tratar de dar respuesta a estas cuestiones, en el seno del 13th International Congress of Antiphospholipid Antibodies, que tuvo lugar en Galvestone en abril de 2010 (Tabla 32), se elaboró un documento de consenso sobre la profilaxis primaria y secundaria en portadores de SAF. La clasificación de diferentes niveles de riesgo mediante parámetros clínicos e inmunológicos (primera trombosis vs evento recurrente, trombosis arterial vs venosa, presencia de lupus eritematoso sistémico [LES] vs SAF no asociado a LES, grado de riesgo del perfil de AAF puede servir de guía para orientar el tratamiento más adecuado a cada paciente, en particular la intensidad y la duración de la anticoagulación.
Entre los diferentes tipos de AAF, el AL es aisladamente el marcador que mejor predice el riesgo trombótico, y el mayor riesgo para trombosis arterial o venosa tiene lugar en pacientes con triple positividad (ACL, AL y anti-2-GP 1). Además, la presencia de AAF es uno de los mayores determinantes para el desarrollo de trombosis en los pacientes con LES.
El sumario de las recomendaciones de tratamiento anti-trombótico en pacientes con SAF se recoge en la tabla 32. Como el propio documento finalmente señala, la mayoría de las recomendaciones se basan en datos débiles o incompletos (niveles de evidencia B o C), siendo deseable por lo tanto, que cualquier modificación a las propuestas de tromboprofilaxis recogidas en el documento se apoye en nuevos estudios con conclusiones de mayor evidencia científica.

Aspectos generales del tratamiento: La experiencia en el tratamiento de pacientes con AAF y fenómenos trombóticos se basa sobre todo en estudios retrospectivos y, por tanto, de un valor limitado.
Tratamiento tras un acontecimiento trombótico: Se ha observado en al menos tres estudios retrospectivos el efecto de anticoagular para descender la recurrencia de trombosis.
El nivel de protección contra trombosis venosas y arteriales se correlaciona directamente con el nivel de anticoagulación. Así, un tratamiento con warfarina (Coumadin®) de intensidad intermedia (INR: 2,0-2,9) o alta (INR igual o superior a 3,0) reduce significativamente la recurrencia de trombosis con respecto a un tratamiento de baja intensidad (INR igual o inferior a 1,9).
El AAS sola es ineficaz en la reducción del rango de recurrencias de trombosis. El clopidogrel (Plavix®) es una alternativa.
Un tratamiento discontinuo con warfarina parece asociarse con un incremento en el riesgo de trombosis e incluso de muerte, sobre todo en los primeros 6 meses tras interrumpir la terapia anticoagulante, por lo que se debe mantener la profilaxis de forma indefinida. Mantener una anticoagulación intermedia o alta es una cuestión que aún no está resuelta (complicaciones hemorrágicas).
No parece ser necesaria la terapia anticoagulante de por vida con acenocumarol/warfarina en pacientes con AAF y un primer episodio de trombosis venosa, puesto que los AAF pueden no estar relacionados con el hecho. La mayoría de expertos recomienda que todos los pacientes con SAF y una trombosis mayor (trombosis arterial o trombosis venosa profunda/embolismo pulmonar) o episodios recurrentes de trombosis, reciban de por vida anticoagulación para mantener un INR mayor o igual a 3,0.
Si a pesar de la terapia anticoagulante hay episodios recurrentes de trombosis, la dosis de acenocumarol/warfarina debe elevarse para subir el INR, o añadir aspirina al tratamiento. Algunos pacientes serán innecesariamente tratados con estas recomendaciones, pero aún no pueden ser identificados. Es habitual en estos pacientes la oscilación de los valores de anticoagulación, debido probablemente a la propia oscilación de los títulos de AAF, por lo que se necesitan controles frecuentes de la coagulación.
Profilaxis en pacientes sin trombosis: De forma general no está recomendada. Se recomienda aspirina (81 mg/día) en pacientes que presentan de forma persistente AAL o títulos altos de AAC del isotipo IgG, especialmente si coexisten otros factores de riesgo trombótico adicionales (HTA, hiperlipidemia, tabaquismo, síndrome nefrótico o sedentarismo, diabetes), o en presencia de anticuerpos anti-B2-glicoproteína 1, aunque no está clara su capacidad de protección. Es importante reducir y evitar cualquier factor que predisponga a trombosis.
Es también necesaria la profilaxis de las trombosis venosas con heparina en pacientes con AAF sometidos a intervenciones quirúrgicas o a encamamiento prolongado y aconsejar a las mujeres no tomar anticonceptivos orales, especialmente con un alto contenido estrogénico.
La hidroxicloroquina puede proteger contra trombosis en pacientes con LES y un SAF secundario.
– Agentes inmunosupresores: No está probada la utilidad de corticoides ni de drogas citotóxicas (ciclofosfamida). Los niveles de AAC parecen ser relativamente resistentes a la terapia inmunosupresora y hay poca evidencia de que estas drogas alteren el curso del estado de hipercoagulabilidad. No obstante, debe considerarse en pacientes que no respondan a la terapia antitrombótica o con ciertos órganos afectados.
Tratamiento en situaciones específicas
– Enfermedad renal: El tratamiento es el mismo tanto si tienen enfermedad renal como si no. Los pacientes con evidencia de trombosis microangiopática en los glomérulos y pequeñas arterias o trombos en las grandes venas deben ser tratados.
En el fallo renal agudo se recomienda, aunque con resultados inciertos, plasmaféresis o corticoides y anticoagulación crónica (INR superior a 3) con o sin bajas dosis de salicilato.
Los pacientes dializados con SAF tienen mayor riesgo de trombosis.
– Trasplante renal: Los pacientes con historia de tromboembolismo y nefritis lúpica, que han progresado a un estadio final de la enfermedad renal, pueden beneficiarse de terapia anticoagulante después del trasplante.
– Embarazo: El tratamiento ha evolucionado considerablemente.
Recientemente se ha visto que la asociación de heparina con dosis bajas de aspirina era más efectiva que la aspirina sola para conseguir nacimientos vivos en mujeres con SAF y pérdidas de embarazos; no obstante, la dosis sigue siendo debatida.
Así, las mujeres con pérdidas preembriónicas y embriónicas recurrentes y sin historia de tromboembolismo deben ser tratadas con 5.000 unidades de heparina dos veces al día, y con dosis mayores si existe historia de tromboembolismo; está menos claro en mujeres con pérdidas durante el periodo fetal pero sin historia de tromboembolismo, aunque se recomienda tromboprofilaxis con 15.000-20.000U de heparina diarias.
Se debe practicar un eco-doppler de la circulación umbilical si aparecen signos de oclusión de la arteria umbilical o sufrimiento fetal, y realizar una inducción del parto o una cesárea si ello ocurre.
– Manifestaciones hematológicas: Los pacientes con SAF y trombocitopenia media no suelen requerir tratamiento. En cambio, no está claro el manejo de una marcada trombocitopenia (alto riesgo de sangrado):
Se han recomendado corticoides y, si es necesario, globulina inmune intravenosa para obtener niveles superiores a 50.000/mm3
- Terapia hormonal (danazol, andrógeno atenuado) y anticoagulación.
- La aspirina a dosis bajas también ha normalizado las plaquetas en algunos pacientes que no responden a esteroides orales.
- Otras posibilidades son dapsona y cloroquina.
– SÍNDROME ANTIFOSFOLÍPIDO CATASTRÓFICO: Una minoría de pacientes (1%) con SAF presenta un síndrome agudo y devastador caracterizado por múltiples oclusiones vasculares simultáneas por todo el organismo, que conduce a la muerte en muchas ocasiones, debido a que son refractarios al tratamiento y con complicaciones asociadas que dificultad el manejo.

Los Criterios Diagnostico del SAF catastrófico se presentan en la Tabla 33. Este se define por la afectación de, por lo menos, tres diferentes órganos sistémicos en un periodo de días o semanas con una histopatología de múltiples oclusiones de grandes o pequeños vasos. Aunque no es frecuente las manifestaciones hemorrágicas en el SAF y de presentarse generalmente existe una condición clínica asociada o es secundaria a anticoagulación, esta descrito la trombocitopenia, el déficit adquirido de protrombina y a la presencia de inhibidores del factor VIII asociadas a AAF que pudiesen favorecer la presencia de sangrados.
En el SAF catastrófico el riñón es más comúnmente afectado (véase Imágenes con fines didácticos), seguido de los pulmones, el sistema nervioso central, el corazón y la piel. En un 25% de los pacientes con este síndrome ocurre coagulación intravascular diseminada (CID). Las manifestaciones microvasculares incluyen microangiopatía trombótica renal, distrés respiratorio del adulto, microinfartos cerebrales y microtrombosis miocárdicas. La mayoría de los pacientes con afectación renal tiene hipertensión, frecuentemente maligna, y requiere diálisis en un 25% de los casos. La muerte ocurre en un 50% de los casos y generalmente es por fallo multiorgánico.
El SAF catastrófico se puede desencadenar por infecciones, retirada de la terapia anticoagulante y uso de fármacos como anticonceptivos orales.
Si se sospecha, se debe realizar plasmaféresis junto con una anticoagulación intensa. La inmunosupresión no da buenos resultados.
Bibliografía
- Fitzpatrick´s Dermatology in General Medicine. Seventh edition. Edited by Wolf; Goldsmith, Katz, Gilchrest, Paller and Leffell. Mc Graw Hill medical publishing división. 2007, chapter 136, 1281-88.
- Juan Antonio Orts, Ángel Zúñiga y María Orera. Actualización del síndrome Antifosfolipídico. Med Clin (Barc) 2003;121(12):459-71.Tettamanti M., Barcia J., Kuhn I., Castillo M., Guerrero Ma. Del Carmen. Vasculitis livedoide en el Síndrome Antifosfolipidico. Gaceta Dermatológica Ecuatoriana. Vol. 2. N 1, Junio 1999.
- Alarcón-Segovia D, Pérez-Vázquez ME, Villa AR, Drenkard C, Cabiedes J. Preliminary classification criteria for the antiphospholipid syndrome within systemic lupus erythematosus. Semin Arthritis Rheum 1992;21: 275-86. 8.
- Silvia S. Pierangeli, Héctor R. Pierangel. Síndrome antifosfolípido: mecanismos patogénicos, diagnóstico y tratamiento. Medicina & Laboratorio, Volumen 14, Números 3-4, 2008.
- Hughes GRV. Thrombosis, abortion, cerebral disease and lupus anticoagulant. BMJ 1983; 287: 1088-9.
- Wilson WA,Gharavi AE,Koike T,et al. International consensus statement on preliminary classification criteria for definite antiphospholipid syndrome: report of an international workshop. Arhtritis Rheum, 42 (1999), pp. 1309-11
- McHugh NJ, Maymo J, Skinner RP, James I, Maddison PJ. Anticardiolipin antibodies, livedo reticularis, and major cerebrovascular and renal disease in systemic lupus erythematosus. Ann Rheum Dis 1988;47:110- 145.
- International Consensus statement on preliminary classification criteria for definitive antiphospholipid síndrome. Wilson et al. Arthritis and Rheumatism 1999;42:1309-1311.
- International consensus statement on an update of the classifi cation criteria for defi nite antiphospholipid syndrome (APS). Miyakis S, Lockshin MD, et al. J Thromb Haemost 2006;4:295-306.
- Rossi Andrea. Catastrophic antiphospholipid syndrome. HEMATOLOGÍA, Vol.18 N° 1: 40-47 Enero – Abril 2014.
- Ruiz-Irastorza G, Cuadrado MJ, Ruiz-Arruza I, Brey R, Crowther M, Derksen R, et al. Evidence-based recommendations for the prevention and long-term manegement of thrombosis in antiphospholipid antibody-positive patients: report of a Task Force at the 13th International Congress on Antiphospholipid Antibodies. Lupus. 2011;20:206—18.
- Sciascia S, Lopez-Pedrera C, Roccatello D, Cuadrado M. Catastrophic antiphospholipid syndrome (CAPS). Best Practic and Research Clínicasl Rheumatology. 2012; 26: 535-541.
- Cervera R, Bucciarelli S, Plasín MA, et al. Catastrophic antiphospholipid syndrome (CAPS): Descriptive analysis of a series of 280 patients from the “CAPS Registry”. J Autoinmun. 2009; 32:240-245.